24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
自2020年新冠疫情爆发以来,国家对医疗器械行业发展重视程度显著提高,在政策方面给予较大支持。国家鼓励创新,从加快器械审批流程、财政税收支持、采购优先选择国货和出台国家级的采购计划等四个方面刺激市场需求,助力医疗器械行业发展。国家正着手加快补齐我国高端医疗器械短板,加快关键核心技术攻关,突破技术装备瓶颈,力争实现高端医疗器械自主可控。医疗器械相关监管部门也在不断的深化医疗体制改革,对医疗器械行业制定了更为细致、明确的监管要求,保障行业发展。
本文基于总体趋势、企业分布、注册信息、市场情况等信息从多维度解析当前人工晶状体医疗器械产品发展趋势和行业现状,旨在客观评价人工晶状体医疗器械产品发展水平和发展质量,为相关企业立项评估、市场调研、投资决策等提供一定数据参考。
1、产品概述
人工晶状体是指人工合成材料制成的一种特殊透镜,它的成分包括硅胶、聚甲基丙烯酸甲酯、水凝胶等。人工晶状体的形状功能与人眼的晶状体相似,具有重量轻、光学性能高、无抗原性、致炎性、致癌性和能生物降解等特性。白内障术后,浑浊的晶状体被摘除,患者眼内植入人工晶状体替代原来的晶状体,此产品可使外界物体在视网膜上聚焦成像,能使患者看清周围景物。
| 07 | 眼科植入物及辅助器械 | 01人工晶状体 | 通常由光学主体和支撑部分组成的光学镜片,其光学区部分通过一定的光学设计从而获取需要的聚焦能力并达到较好的成像质量。 | 代替人眼晶状体,用于囊外摘除术的白内障手术后或超声乳化术后植入,矫正或修正人眼视力。 | 人工晶状体、肝素表面处理亲水性丙烯酸人工晶状体、亲水性丙烯酸人工晶状体、虹膜夹无晶体眼人工晶状体、预装式非球面后房人工晶状体、折叠式非球面人工晶状体、折叠式多焦丙烯酸人工晶状体、着色非亲水丙烯酸非球面后房人工晶状体、后房型聚甲基丙烯酸甲酯人工晶状体、单件式多焦复曲面人工晶状体、一件式后房型人工晶状体、三件式后房型人工晶状体、后房人工晶状体、折叠式人工晶状体、单件式多焦人工晶状体、折叠式后房硅凝胶人工晶状体、有晶体眼屈光性人工晶状体、折叠式后房人工晶状体、聚甲基丙烯酸甲酯人工晶状体、亲水性丙烯酸酯非球面人工晶状体、肝素表面处理聚甲基丙烯酸甲酯人工晶状体、肝素表面处理亲水性丙烯酸非球面人工晶状体、单件式复曲面人工晶状体、聚丙烯酸酯类后房型人工晶状体、折叠式后房丙烯酸人工晶状体、可调节人工晶状体、预装式人工晶状体、折叠式丙烯酸人工晶状体、非亲水丙烯酸后房人工晶状体、一件式人工晶状体、后房人工晶体、后房型丙烯酸酯人工晶状体、单件式疏水性丙烯酸人工晶状体、非球面后房人工晶状体、单件式黄色疏水性丙烯酸人工晶状体、前房型聚甲基丙烯酸甲酯人工状晶体、多焦聚丙烯酸酯类后房人工晶状体、后房型屈光晶状体、有晶体眼后房屈光晶状体、带虹膜的人工晶状体 | Ⅲ |
2、产品注册
2.1总体趋势
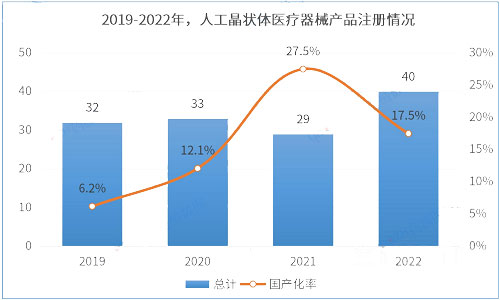
截至2023年7月,人工晶状体医疗器械产品在有效期内产品注册总数为151件。其中,国产产品有27件,占比17.8%。2019-2022年注册数量总体呈上升趋势,其中超过半数注册产品为进口注册,2022年国产占比率为17.5%。
2.2人工晶状体医疗器械产品注册形式
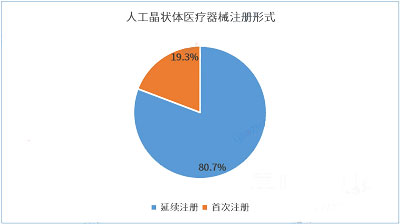
从产品注册形式来看,截至2023年7月,在有效期内人工晶状体医疗器械产品首次注册数量为29项,延续注册产品数量为122项。
2.3人工晶状体医疗器械产品国产&进口产品注册情况
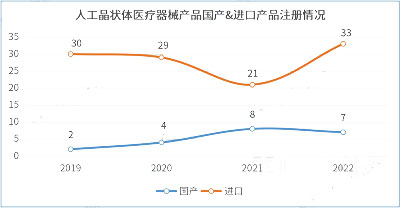
据统计,截至2023年7月,人工晶状体医疗器械进口注册产品数量领先于国产注册产品,四年国产化率在15.8%左右。
2.4国产人工晶状体医疗器械产品注册省份分布情况
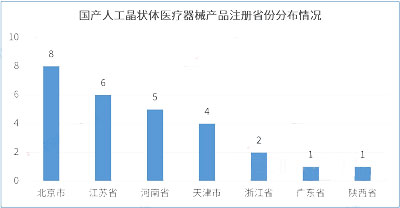
截至2023年7月,共有7个省份(不包括中国港澳台)注册人工晶状体医疗器械产品,北京市国产产品注册数量排名第一,产品注册数为8件,占国产产品总数的38.0%。剩下排名前三的省份依次是:江苏省6件,河南省5件。
2.5国产人工晶状体医疗器械产品注册人情况
据统计,截至2023年7月,国内共有10家企业注册国产人工晶状体医疗器械产品,注册数量排名第一的企业是位于北京市的爱博诺德(北京)医疗科技股份有限公司,产品注册数为8件。

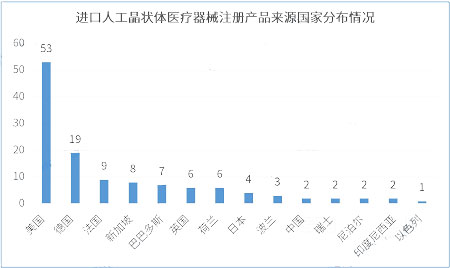
2.6进口人工晶状体医疗器械注册产品来源国家分布情况
据统计,截至2023年7月,14个国家在我国境内注册人工晶状体医疗器械产品共124件。注册产品数量最多的国家是美国53件,占进口产品总量的42.7%。
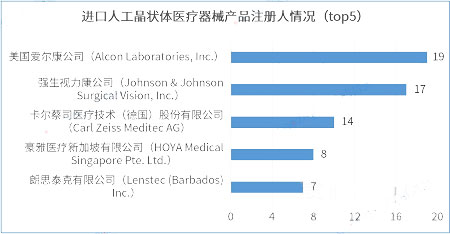
2.7进口人工晶状体医疗器械产品注册人情况(top5)
据统计,截至2023年7月,进口人工晶状体医疗器械产品注册数量排名第一的企业是美国的美国奇亿娱乐康公司(Alcon Laboratories, Inc.),产品注册数为19件。
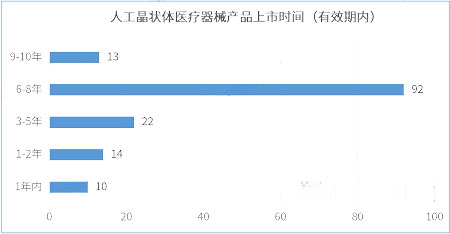
2.8人工晶状体医疗器械产品上市时间
据统计,从产品进入市场的平均时间来看,在有效期内的人工晶状体医疗器械产品的上市时间在6-8年的产品数量最多,有92件。
3、市场情况
3.1生产企业
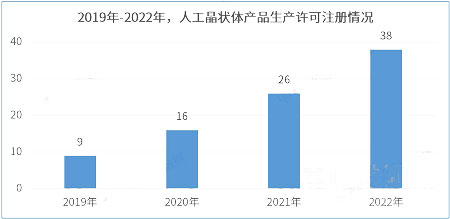
据统计,截至2023年3月,全国可生产人工晶状体医疗器械产品的生产企业共有64家。2022年注册人工晶状体医疗器械产品生产许可企业数量最多,有38家。
3.2人工晶状体产品生产企业省份分布情况
据统计,从人工晶状体产品生产企业省份分布情况来看,上海市与山东省可生产人工晶状体医疗器械产品的生产企业数量排名并列第一,均为9家。剩余排名前三的省份依次是:江苏省8家,湖南省与浙江省各5家。

4、小结
从产品注册情况来看,2019-2022年注册数量总体呈上升趋势,四年国产占比率在15.8%左右,其中有效期内首次注册人工晶状体医疗器械占19.3%。
从产业规模来看,目前我国注册人工晶状体医疗器械产品数量最多的省份是北京市,占国产注册数量的38.0%,进口产品主要来源于美国,占进口产品的42.7%。
从我国人工晶状体医疗器械市场情况来看,生产企业数量逐年上升,主要集中在上海市、山东省、江苏省等省市。目前人工晶状体医疗器械有效产品数量最多的生产企业是位于北京市的爱博诺德(北京)医疗科技股份有限公司,产品注册数为8件。
目前来看,人工晶状体医疗器械产品主要依赖于进口产品,国产替代率较低。2023年5月国务院新闻办公室举行“权威部门话开局”系列主题新闻发布会上,据国家医疗保障局介绍,即将开展的第四批高值医用耗材的国采,将主要聚焦于眼科的人工晶体和骨科的运动医学类耗材,在此之前,各省份均已开启人工晶体省级集中带量采购,2022年1月,天津市医保局牵头组织京津冀“3+N”奇亿娱乐人工晶体、药物球囊和起搏器类医用耗材集采工作,其中14个省份参加人工晶体集采。人工晶体在去年平均降幅46.4%的基础上,再次降低16.91%,平均价为2347元/片,未来人工晶体仍有降价空间。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
奇亿娱乐(中国)有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。