24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
近期,急速医疗有限公司荣幸宣布其研发的“颅内取栓支架”已经获得上市批准。在此,奇亿娱乐CRO(临床研究外包合作伙伴)将与您一同深入了解这一医疗创新产品在临床前研发阶段所经历的实验过程。
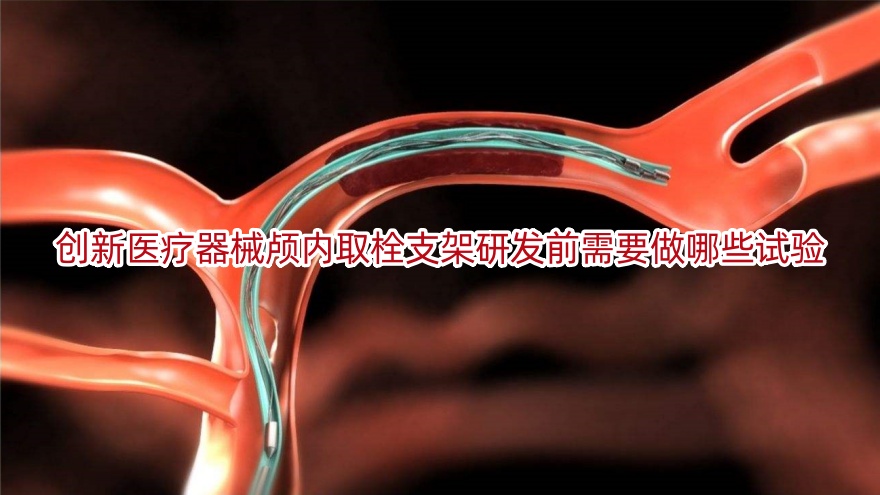
1. 颅内取栓支架的构造和组成
这一产品由多个部分组成,包括头端、编织丝网、推送轴、控制丝和手柄等。编织丝网的核心材料为带有钽芯的镍钛丝,而近端和远端分别装有90%铂和10%铱合金的显影标记。该产品通过环氧乙烷灭菌处理,为一次性使用,货架有效期为2.5年。
2. 颅内取栓支架的应用范围
该产品旨在用于在症状发作8小时内移除缺血性脑卒中患者颈内动脉、大脑中动脉M1和M2段以及基底动脉中的血栓,从而恢复血流。该治疗不适用于使用静脉组织型纤溶酶原激活物(IVt-PA)或IVt-PA治疗失败的患者。
3. 颅内取栓支架的工作原理

这一产品的主要目标是在局部捕获脑血栓,并将其移除,从而重建血流。产品在射线透视下通过微导管输送至病变部位,然后释放编织丝网至目标血管中的血栓处。编织丝网能够在出微导管时保持其原始收缩尺寸,以确保准确性。在编织丝网位置确定后,操作者可以通过手柄展开编织丝网,根据需要调整直径和径向支撑力。完成嵌栓后,编织丝网可以适度收缩,以减少径向支撑力并降低对血管的损伤风险。
4. 颅内取栓支架的性能研究
表 1 产品技术要求研究摘要
| 序 号 | 研究项目 | 验证结论 |
| 1 | 外观 | 合格 |
| 2 | 产品尺寸 | 合格 |
| 3 | 抗拉强度 | 合格 |
| 4 | 抗扭结性 | 合格 |
| 5 | 径向支撑力 | 合格 |
| 6 | 模拟使用 | 合格 |
| 7 | 输送、释放和回撤力 | 合格 |
| 8 | 耐腐蚀性 | 合格 |
| 9 | 微粒 | 合格 |
| 10 | 编织丝网相变温度 | 合格 |
| 11 | 化学性能 | 合格 |
| 12 | 还原物质 | 合格 |
| 13 | 重金属含量 | 合格 |
| 14 | 酸碱度 | 合格 |
| 15 | 蒸发残渣(不挥发物) | 合格 |
| 16 | 紫外吸收度 | 合格 |
| 17 | 环氧乙烷残留量 | 合格 |
| 18 | 无菌 | 合格 |
| 19 | 细菌内毒素 | 合格 |
在产品研发过程中,进行了一系列的性能研究,涵盖了结构要求、可视性、控制丝涂层完整性、模拟使用后微粒和疲劳等。这些研究结果表明,产品符合设计输入要求。
5. 颅内取栓支架的生物相容性研究
由于该产品与循环血液短期接触,因此进行了生物相容性评价。根据相关标准,对产品的生物相容性风险进行了评估,结果表明其风险是可接受的。
表 2 生物相容性试验项目
| 评价项目 | 申报产品 |
| 热原 | √ |
| 细胞毒性 | √ |
| 致敏 | √ |
| 皮内反应 | √ |
| 急性全身毒性 | √ |
| 溶血 | √ |
| 补体SC5b-9 | √ |
| 体内血栓形成 | √ |
| 部分凝血激活酶时间 | √ |
6. 颅内取栓支架的灭菌研究
为确保产品的无菌状态,采用了环氧乙烷灭菌方法,并通过灭菌过程确认,确保无菌保证水平为10^-6。
7. 颅内取栓支架的有效期和包装研究
产品的货架有效期为2.5年,开发人员进行了相关研究,对包装系统进行了加速老化奇亿娱乐时老化研究,确保产品的稳定性和完整性。
8. 颅内取栓支架的动物研究
为确认产品在动物模型中的可行性和安全性,开发人员进行了动物研究。结果表明,产品达到了预期设计要求。
这一系列实验和研究为“颅内取栓支架”的临床应用奠定了坚实的基础,也为脑卒中患者的治疗提供了新的奇亿娱乐。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
奇亿娱乐(中国)有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。