24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
本文分享两个常见问题:一个是常见考题:实施GCP的利弊有哪些?另一个是研究者比较关心的问题:GCP对参加试验的研究者有哪些要求?
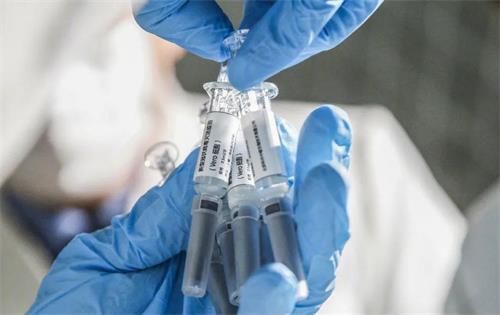
(1)利
受试者可得到更好的保护;
只有合格的研究者及研究基地才能进行临床试验,从而可确保临床试验的质量;
试验数据更准确、真实、可信;
GCP可促进申办者和研究者更好的培训并提高两者的技术水平;
GCP和标准操作程序的实施可使制药企业内部及企业之间的试验操作得以统一;
一套完整的试验文档保证了试验的透明度和可靠的质量;
管理当局对一贯严格遵守GCP的申办者的信任程度增强;
如按ICHGCP的要求,资料可用于全球注册;
节约研发及申报时间,产品可尽快上市;
良好的开端会收到事半功倍的效果。
(2)弊
要求研究者、申办者和监查员付出更多的时间和奇亿娱乐进行临床试验;
研究者会感觉到监查工作繁琐费时,如病例报告表的改正过程、监查员的访视及稽查等;
CRA和研究部门不能直接管理试验,因此不能直接保证临床试验的进度并控制试验的质量;
由于GCP要求保留试验资料时间较长,3年、5年甚至15年,造成试验资料归档和保管的困难;
试验费用增加。
具备完成特定试验所须的教育、培训和经验,包括业务及GCP方面的知识;
熟悉试验用药品的特性及用法;
熟悉试验方案,并保证严格按照方案实施临床试验,必要时可参与试验方案的修订;
协助申办者在试验开始前获得伦理委员的批准;
负责获得受试者签字的知情同意书;
确保试验点具备良好条件,包括足够的人员和适当的设施;
具备充足的病源以保证按时完成受试者入组;
有足够的时间保质、按时完成试验。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
奇亿娱乐(中国)有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。