24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

授权分工表是临床启动会中最重要的工作之一,临床试验的主要研究者对整个项目负责,但由于主要研究者较忙,“往往”没时间面面俱到,因此需要授权给项目组各成员分工协作,完成整个临床试验。启动会中,由主要研究者亲自填写授权分工,各被授权的研究者签名。授权分工表可以采用各中心模板,但建议自制以便各中心统一模板。

请注意如下要点:
(1)授权分工表必须保留原件;
(2)分工职责需明确,一项工作授权给多人,也可仅一人负责;
(3)若启动会某医生未能参加,可后面补授权,但必须有培训记录。
(4)各研究者需了解工作内容及要求,便于CRC协助各研究者开展工作;
(5)可新增科室医生,新授权前需要有培训记录,注意培训日期。
授权分工表形式各种各样,但究其内容不会有太大差异,内容包括:
(1)临床试验方案名称、编号;
(2)试验中心、编号;主要研究者、科室;
(3)授权开始时间、结束时间;
(4)分工职责包括:获取知情同意、受试者筛选/随机、收集/评估相关医学报告、试验操作及原始数据记录、试验产品管理、CRF填写、文件管理、其他等。
授权分工样表如下:
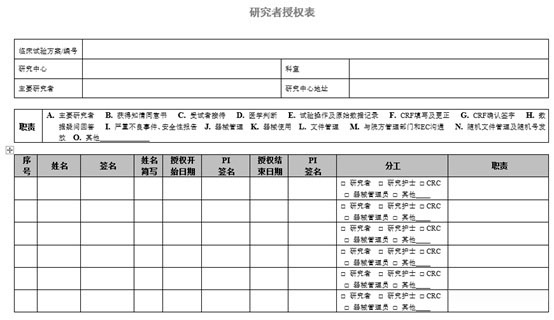
样表1
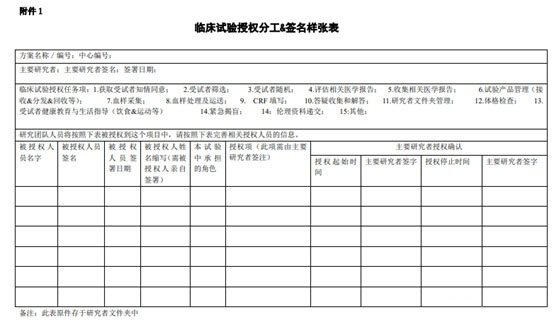
样表2
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
奇亿娱乐(中国)有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。